Materiales de Apoyo
Última innovación en Infatrini, ahora con HMO
Infatrini, líder* en la recuperación del crecimiento y el desarrollo, es la fórmula para lactantes más cercana a la leche materna por su mezcla prebiótica única scGOS/lcFOS (9:1) que imita la cantidad, diversidad y funcionalidad de los oligosacáridos de la leche materna (HMO)1-6, promoviendo el crecimiento de bacterias beneficiosas, fortaleciendo7-8 la barrera intestinal y evitando la adhesión y crecimiento de patógenos.10-14
Aporta, además, el mayor contenido en nucleótidos de las fórmulas para lactantes.
Ahora, Infatrini va un paso más allá acercándose aún más a la leche materna ya que contiene 2’FL, el HMO más abundante, que junto con la mezcla prebiótica única scGOS/lcFOS (9:1) favorece un efecto sinérgico inmunomodulador15-17 que ayuda a reforzar el sistema inmune en pacientes pediátricos con compromiso del crecimiento.
Se estima que la tasa de desnutrición entre los niños con CC oscila entre el 15-64% 18
El estado nutricional de los lactantes con CC se ve gravemente comprometido durante todo el periodo anterior y posterior a la cirugía. (19-24)
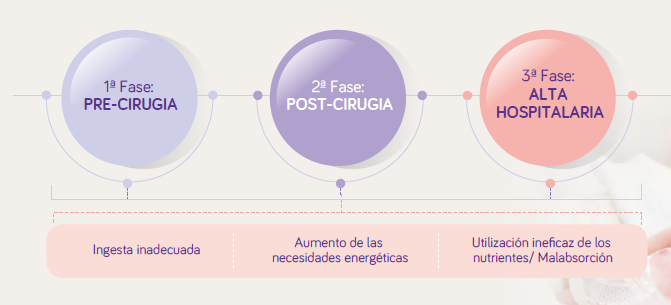
La SEGHNP y SECPCC recomiendan utilizar una fórmula polimérica líquida de nutrición enteral hipercalórica para lactantes. (25)
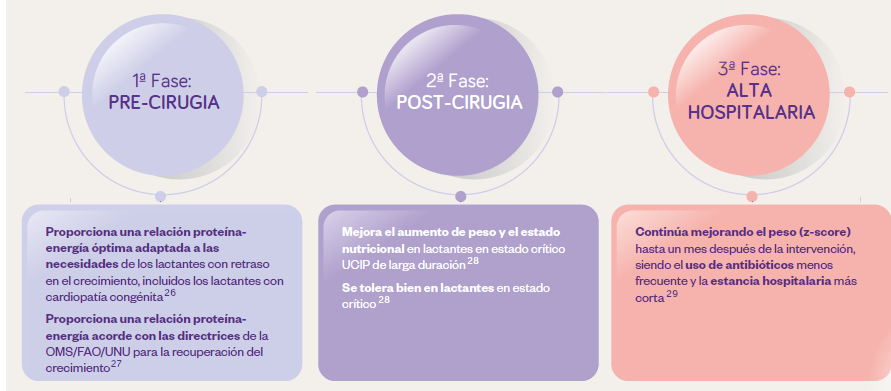
El uso de Infatrini en lactantes con CC mejora el crecimiento contribuyendo en una mejora de los resultados clínicos en las cirugías (28,29)
Recopilación de experiencias clínicas en pacientes con patologías diversas (cardiopatías congénitas, enfermedades pulmonares, prematuridad, parálisis cerebral, malformaciones orofaciales, atresia de esófago, hepatopatías y epidermólisis ampollosa) que han necesitado el uso de una fórmula hipercalórica.
Casos Clínicos Infatrini


Referencias:
*IQVIA data nutrición enteral para lactantes MAT. Junio 2024
1. Salminen S. et al. Nutrients. 2020 Jun 30;12(7):1952.
2. Reverri et al. Nutrients, 2018;10:1346
3. Azagra-Boronat I, et al. Front. lmmunol. 2019;8(8):876.
4. Xiao L, et al. J Nutr, 2019;149(5):856–69.
5. De Kivit S, et al. J Innate lmmun. 2013;5(6):625–38.
6. Boehm G, et al. Acta Paediatr Suppl. 2003;91(441):64-7.
7. Knol J, et al. British Journal of Nutrition. 2005;94:783–90.
8. Moro G, et al. J Pediatr Gastroenterol Nutr. 2002;34:291–5.
9. Yu ZT, et al. J Nutr. 2016;146(10):1980-90.
10. Ruiz-Palacios GM, et al. J of Biol Chem. 2003;278(16):14112-20.
11. Weichert S, et al. Nutrition Research. 2013;33(10):831-8.
12. De Kivit S, et al. J Innate lmmun. 2013;5(6):625–38.
13. Bruzzese E, et al. Clinical Nutrition. 2009;28:156–61.
14. Knol J, et al. J Pediatr Gastronterol Nutr. 2003;36:566.32.
15. Lehmann S, et al. PLoS One. 2015;10(7):e0132304.
16. Overbeek LS, et al. J Pediatr Gastroenterol Nutr. 2019;68(S1).
17. Salminen S, et al. Eds. The Biotics Family in Early Life. Chichester, UK: John Wiley and Sons Ltd, 2023.
18. Larson-Nath C, Goday P. Nutr Clin Pract. 2019;34:349-58.
19. Roman B. Pract Gastroenterol. 2011;8:11-32.
20. Steltzer M. et al. Clinics in perinatoloy. 2005;32(4):1017-30.
21. Norris MK, Hill CS. Crit Care Nurs Clin North Am. 1994;6:153-63.
22. Leitch CA. Pro Pediatr Cardiol. 2000;11:195-202.
23. McGrail K. Topics in Clinical Nutrition. 1997;13(1):62-8.
24. Anderson JB. et al. Ann Thorac Sur. 2011;91:1460-6.
25. Centeno-Malfaz F, et al. Anales de Pediatría 98 (2023) 373×383.
26. Clarke, S. E. et al. J Hum Nutr Diet. 2007;20(4), 329-339.
27. Protein and amino acid requirements in human nutrition. Report of a joint FAO/WHO/UNU expert consultation, WHO 2007.
28. Eveleens, RD. et al. J Hum Nutr Diet. 2018.
29. Scheeer VA. et al. JPEN J Parenter Enteral Nutr. 2019 Mar 22.


